Mit der Veröffentlichung der neuen Revision des EU-GMP-Annex 1 ist eine Überprüfung der derzeitigen Praktiken erforderlich, um sicherzustellen, dass das installierte Überwachungssystem, das zur Erfüllung der Anforderungen von Annex 1 ausgewählt wurde, die Anforderungen erfüllt. In diesem Kapitel werden die Anforderungen von Annex 1 anhand der derzeit installierten Systeme überprüft.
Reinraumklassifizierung
Pharmazeutische Reinräume werden nach der Partikelkonzentration in der Luft klassifiziert, die erforderlich ist, um die Reinheitskriterien für den durchgeführten Herstellungsprozess zu erfüllen. Die Bestimmung der Reinraumklasse ist ein Prozess, der auf tatsächlichen statistisch validen Messungen beruht und eine Funktion des Filter- und Betriebsstatus des Raums ist. Es handelt sich im Wesentlichen um eine Kalibrierung des Raums, um sicherzustellen, dass er die vorgesehene Klassifizierung erfüllt, und nicht in erster Linie um eine Funktion des Anwendungsrisikos [2].
Bei der Partikelzählung in Reinräumen gibt es drei Messphasen:
As Built: ein fertiggestellter Raum mit allen angeschlossenen und funktionsfähigen Diensten, aber ohne Produktionsausrüstung oder Personal in der Einrichtung.
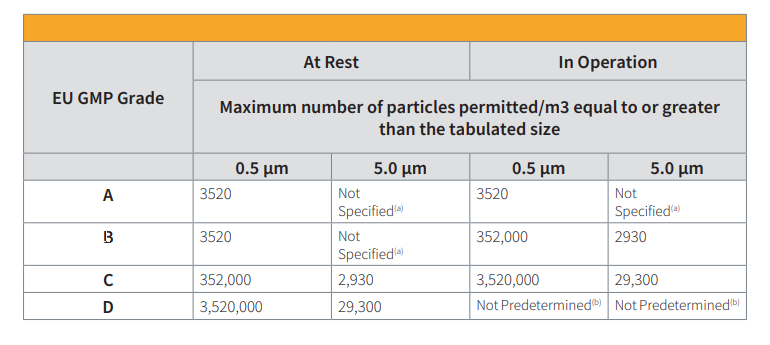
Im Ruhezustand: Alle Dienste sind angeschlossen, die gesamte Ausrüstung ist installiert und funktioniert nach einem vereinbarten Verfahren, aber es ist kein Personal anwesend.
In Betrieb: Die gesamte Ausrüstung ist installiert und funktioniert in einem vereinbarten Format, und es ist eine bestimmte Anzahl von Mitarbeitern anwesend, die nach einem vereinbarten Verfahren arbeiten.
